- आवर्त सारणी के उपवर्ग में 4 ए का सदस्य है।
- कार्बन का संकेत - सी
- परमाणु संख्या - 6
- इलेक्ट्रॉनिक विन्यास - 1s22s22p2
- संयोजी इलेक्ट्रॉनों की संख्या - 4
- किसी तत्त्व के दो या दो से अधिक रूप जो गुणधर्मों में एक-दूसरे से पर्याप्त भिन्न होते हैं, अपररूप कहलाते हैं तथा इस गुण को अपररूपता कहते हैं।
- कार्बन प्रकृति में विभिन्न अपरुपों में पाया जाता है। इनके भौतिक गुणधर्म व व्यवहार भिन्न होते हैं।
- कार्बन मुक्त अवस्था में हीरा, ग्रेफाइट तथा कोयले के रूप में पाया जाता है।
- कार्बन वर्ग के तत्वों में लेड को छोड़कर सभी अपरूपता का गुण प्रदर्शित करते हैं।
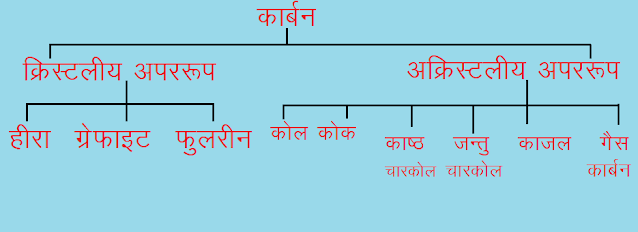
क्रिस्टलीय अपररूप -
- वह अपररूप जिसमें कार्बन परमाणु एक निश्चित व्यवस्था में व्यवस्थित रहते हुए एक निश्चित ज्यामिति से निश्चित बन्धकोण का निर्माण करते हैं, क्रिस्टलीय अपररूप कहलाते हैं।
हीरा
- हीरे में कार्बन का प्रत्येक कार्बन परमाणु के चार अन्य परमाणुओं के साथ आबंधित होकर एक दृढ़ त्रिआयामी चतुष्फलकीय संरचना का निर्माण करता है।
- यह कार्बन का अतिशुद्ध रूप है।
- इसमें कार्बन-कार्बन के मध्य बन्ध दूरी 1.54 A0 होती है।
- ये विद्युत के कुचालक होते हैं क्योंकि कार्बन की चारों संयोजकताएं चार अन्य कार्बन परमाणुओं से जुड़ी होती है अतः मुक्त इलेक्ट्रॉन नहीं होते हैं।
- हीरे की संरचना में प्रबल सहसंयोजक बंधों का त्रिविम जाल होता है। अतः यह अत्यधिक कठोर होता है। हीरा अब तक का ज्ञात सर्वाधिक कठोर पदार्थ है।
- हीरे का गलनांक 3843 k होता है।
- कोयले की परतों पर चट्टानों का दाब पड़ने से हीरा पारदर्शक हो जाता है।
- शुद्ध कार्बन को अत्यधिक उच्च दाब एवं ताप पर उपचारित (subjecting) करके हीरे को संश्लेषित किया जा सकता है।
हीरे का उपयोग
- कांच को काटने में कटर के रूप में
- चट्टानों एवं पत्थर काटने की मशीन में इसका उपयोग होता है।
- फोनोग्राम की सुई बनाने में।
- कई रत्नों, आभूषणों के निर्माण में हीरे का उपयोग होता है।
ग्रेफाइट
- ग्रेफाइट ग्रेफो शब्द से बना है जिसका अर्थ होता है लिखना।
- ग्रेफाइट में कार्बन का प्रत्येक परमाणु कार्बन के तीन अन्य परमाणुओं के साथ एक ही तल में बनाते हुए षट्कोणीय वलय संरचना बनाते हैं। इनमें से एक बन्ध द्विबंधी होता है। जिससे कार्बन की संयोजकता पूरी होती है।
- ग्रेफाइट की संरचना में षट्कोणीय तल एक-दूसरे के ऊपर व्यवस्थित होकर परत संरचना का निर्माण करते हैं।
- दो परतों के मध्य दुर्बल बन्ध होने तथा उनके मध्य दूरी अधिक होने से एक परत दूसरी परत पर फिसल सकती है। यही कारण है कि ग्रेफाइट को शुष्क स्नेहक के रूप में प्रयुक्त करते हैं।
- मुक्त इलेक्ट्रॉनों की उपस्थिति एवं दो परतों के मध्य उपस्थित स्थान के कारण ग्रेफाइट विद्युत का सुचालक होता है।
- ग्रेफाइट काले धूसर रंग का मुलायम पदार्थ होता है।
- ग्रेफाइट चिकना तथा फिसलनशील पदार्थ होता है।
- यह चमकीला पदार्थ होता है।
उत्तक
फलों व सब्जियों के खाने योग्य भाग
ग्रेफाइट के उपयोग
- ग्रेफाइट पेंसिल में प्रयुक्त होता है।
- शुष्क स्नेहक के रूप में काम आता है।
- इलेक्ट्रॉड बनाने में काम आता है।
- लोहे की वस्तुओं पर पॉलिश के काम
- नाभिकीय परमाणु भट्टी में मंदक के रूप में
फुलरीन
- फुलरीन की संरचना एक फुटबाल की तरह होती है।
- अमेरिका के प्रसिद्ध वास्तुकार बकमिन्सटर फुलर के नाम पर इसका नाम फुलरीन रखा गया।
- फुलरीन के अणु में 60, 70 या अधिक कार्बन परमाणु भी पाए जाते हैं।
- C60 सर्वाधिक स्थायी फुलरीन है जिसे बकमिन्सटर फुलरीन भी कहते है।
- C60 की संरचना में 32 फलक होते हैं जिसमें 20 फलक षट्कोणीय तथा 12 फलकपंचकोणीय होते हैं। इसकी संरचना फुटबॉल के समान होती है। अतः इसे ‘बकीबॉल’ भी कहा जाता है।
- C60 विद्युत का कुचालक होता है एवं इसमें कार्बन-कार्बन बंध की लम्बाई 1.40 A0 होती है।
- फुलरीन गोल गुम्बद के समान लगते हैं।
फुलरीन के उपयोग
- प्राकृतिक गैस के शुद्धिकरण में
- आण्विक बेयरिंग में
- उच्च ताप पर अतिचालक होने के कारण तकनीकी रूप से यह कार्बन का महत्त्वपूर्ण अपररूप है।